Priony – patologiczne białka, które niszczą mózg
Autorka: Luiza Łuniewska
Nie są wirusami ani bakteriami, a mimo to zabijają. Priony – patologiczne białka – odpowiadają za grupę zawsze śmiertelnych chorób mózgu i od lat stanowią jedno z największych wyzwań współczesnej neurologii. Najnowsze odkrycia pokazują, że ich znaczenie wykracza daleko poza rzadkie encefalopatie.
W biologii i medycynie niewiele jest zjawisk tak dziwnych jak priony. Przez dekady obowiązywało przekonanie, że choroby zakaźne wywołują wyłącznie organizmy zawierające materiał genetyczny – bakterie, wirusy czy pasożyty. Tymczasem priony burzą ten porządek. Są wyłącznie białkami, a mimo to potrafią „zarażać”, namnażać się i prowadzić do śmiertelnych chorób mózgu. Co więcej, mechanizmy ich działania okazują się kluczowe także dla zrozumienia innych, znacznie częstszych chorób neurodegeneracyjnych.
Białko, które staje się patogenem
Termin „prion” został wprowadzony w latach 80. XX wieku przez Stanleya B. Prusinera, amerykańskiego neurologa i biochemika, który jako pierwszy sformułował i udowodnił hipotezę białkowego czynnika zakaźnego. Odkrycie to – początkowo przyjmowane z dużym sceptycyzmem – przyniosło mu Nagrodę Nobla w 1997 roku i na trwałe zmieniło sposób myślenia o patogenach.
Historia odkrycia prionów pokazuje, jak trudne bywa przełamywanie naukowych paradygmatów. Gdy pojawiła się hipoteza, że czynnik zakaźny może nie zawierać żadnego materiału genetycznego, spotkała się ona z ostrą krytyką. Dominujące wówczas podejście wirusologiczne nie dopuszczało możliwości istnienia „gołego” białka zdolnego do przenoszenia choroby. Przełom nastąpił dopiero wtedy, gdy kolejne eksperymenty wykazały, że infekcyjność preparatów prionowych utrzymuje się mimo niszczenia DNA i RNA, natomiast zanika po degradacji białka. Dziś ten epizod bywa przywoływany jako klasyczny przykład tego, że fundamentalne odkrycia wymagają zakwestionowania najbardziej oczywistych założeń.
Normalne białko prionowe, określane jako PrPᶜ, występuje naturalnie w komórkach nerwowych i innych tkankach. Jego dokładna funkcja biologiczna nie jest do końca poznana, jednak uważa się, że może uczestniczyć w procesach sygnalizacji komórkowej oraz chronić neurony przed stresem oksydacyjnym. Problem pojawia się w momencie, gdy białko to zmienia swoją strukturę przestrzenną. Patologiczna forma, PrPˢᶜ, przyjmuje inną konformację, bogatą w struktury beta, co czyni ją wyjątkowo stabilną i skłonną do tworzenia nierozpuszczalnych agregatów.
Zakażenie bez genów
To, co czyni priony wyjątkowymi, to sposób ich „rozmnażania”. Nie kopiują one informacji genetycznej, lecz działają jak matryca konformacyjna. Patologiczne białko oddziałuje z prawidłową formą PrPᶜ i wymusza na niej zmianę struktury, przekształcając ją w kolejną cząsteczkę PrPˢᶜ. Proces ten prowadzi do lawinowego narastania agregatów, które gromadzą się w tkance mózgowej i zaburzają funkcjonowanie neuronów.
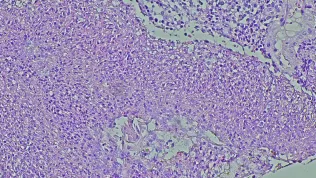
Badania molekularne pokazują, że to właśnie agregacja błędnie sfałdowanych białek jest głównym źródłem neurotoksyczności. Z czasem dochodzi do obumierania komórek nerwowych, a w obrazie mikroskopowym mózg chorego przyjmuje charakterystyczny, gąbczasty wygląd. Od tego obrazu pochodzi nazwa całej grupy schorzeń: pasażowalne encefalopatie gąbczaste.
U ludzi choroby prionowe należą do rzadkich, ale mają zawsze śmiertelny przebieg. Najczęściej rozpoznawaną jest choroba Creutzfeldta-Jakoba, która w większości przypadków występuje sporadycznie, bez uchwytnej przyczyny. Rzadziej spotyka się postacie genetyczne, związane z mutacjami w genie PRNP, oraz formy nabyte, wynikające z kontaktu z materiałem zakaźnym.
Z klinicznego punktu widzenia są to choroby szczególnie trudne diagnostycznie. Wczesne objawy bywają niespecyficzne i obejmują zaburzenia pamięci, zmiany osobowości, problemy z koordynacją ruchową czy zaburzenia mowy. Dopiero szybka progresja objawów i charakterystyczne zmiany w badaniach dodatkowych naprowadzają lekarzy na właściwe rozpoznanie. To sprawia, że pacjenci i ich bliscy często przez długi czas pozostają w niepewności diagnostycznej.
Inne, znacznie rzadsze choroby prionowe to zespół Gerstmanna-Sträusslera-Scheinkera oraz śmiertelna bezsenność rodzinna, w której dominują postępujące zaburzenia snu i funkcji autonomicznych. Szczególne miejsce w historii medycyny zajmuje także kuru – choroba opisana wśród rdzennych mieszkańców Papui-Nowej Gwinei, związana z rytualnym kanibalizmem. Jej wygaszenie po zaprzestaniu tych praktyk stało się jednym z najmocniejszych dowodów na zakaźny charakter prionów.
Priony u zwierząt i ryzyko dla ludzi
Prionowe choroby zwierząt, takie jak scrapie u owiec, gąbczasta encefalopatia bydła czy chronic wasting disease u jeleniowatych, odgrywają istotną rolę w badaniach nad epidemiologią prionów. Szczególny niepokój budzi ta ostatnia, ponieważ rozprzestrzenia się szeroko w populacjach dzikich zwierząt i wykazuje zdolność długotrwałego utrzymywania się w środowisku.
Badania wykazały, że priony odpowiedzialne za chronic wasting disease mogą pozostawać zakaźne w glebie przez wiele lat. Oznacza to, że nawet po eliminacji chorych osobników ryzyko dalszego szerzenia się choroby nie znika. Choć dotychczas nie potwierdzono jednoznacznie przeniesienia tej choroby na ludzi, eksperci podkreślają, że historia epidemii gąbczastej encefalopatii bydła uczy ostrożności. Bariery międzygatunkowe nie są absolutne, a zdolność prionów do adaptacji wymaga stałego monitorowania.
Diagnostyka prionów: przełom ostatnich lat
Jeszcze kilkanaście lat temu rozpoznanie choroby prionowej było możliwe niemal wyłącznie pośmiertnie. Przełom przyniósł rozwój techniki RT-QuIC, która pozwala wykrywać śladowe ilości patologicznego białka prionowego w płynie mózgowo-rdzeniowym, a w niektórych przypadkach także w krwi czy skórze. Metoda ta charakteryzuje się bardzo wysoką czułością i swoistością.
Eksperci podkreślają, że nowoczesna diagnostyka ma znaczenie nie tylko kliniczne, ale także etyczne i psychologiczne. Wcześniejsze i pewniejsze rozpoznanie pozwala uniknąć niepotrzebnych procedur oraz umożliwia pacjentom i ich rodzinom świadome planowanie opieki paliatywnej.
Mimo ogromnego postępu w diagnostyce, medycyna nadal nie dysponuje skuteczną terapią chorób prionowych. Badania koncentrują się dziś na próbach zahamowania agregacji białka prionowego, modulacji ekspresji genu PRNP oraz ochronie neuronów przed toksycznymi skutkami nagromadzonych agregatów.
Coraz większe zainteresowanie budzą strategie polegające na obniżaniu poziomu prawidłowego białka prionowego w mózgu. Badania na modelach zwierzęcych sugerują, że zmniejszenie jego ekspresji może znacząco opóźniać rozwój choroby. Równolegle trwają prace nad cząsteczkami stabilizującymi prawidłową strukturę białka i blokującymi jego patologiczne interakcje. Największym wyzwaniem pozostaje jednak fakt, że w momencie pojawienia się objawów klinicznych uszkodzenie mózgu jest już bardzo zaawansowane.
W ostatnich latach priony stały się ważnym modelem badawczym także dla innych chorób neurodegeneracyjnych. Coraz więcej danych wskazuje, że białka związane z chorobą Alzheimera, Parkinsona czy stwardnieniem zanikowym bocznym wykazują właściwości prionopodobne – zdolność do rozprzestrzeniania się patologicznych konformacji w mózgu.
Z perspektywy współczesnej neurologii priony przestały być traktowane jako rzadkie i egzotyczne patogeny. Stały się kluczem do zrozumienia procesów fałdowania białek, ich agregacji i szerzenia się patologii w sieciach neuronalnych. Paradoksalnie to właśnie one – jedne z najbardziej bezwzględnych wrogów mózgu – dostarczają dziś wiedzy, która może w przyszłości pomóc w walce z chorobami dotykającymi milionów ludzi na całym świecie.