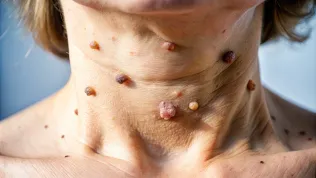
Choroby spichrzeniowe i choroba Alzheimera. Może być jeden lek?
Autorka: Beata Igielska
Ekspert: Prof. Grzegorz Władysław Węgrzyn, genetyk,
A gdyby tak znaleźć lek, który leczyłby nie jedną chorobę, a wiele – zarówno neurodegeneracyjne, jak i tzw. spichrzeniowe, w których wskutek mutacji genetycznej komórki stopniowo przestają prawidłowo działać? Zdaniem prof. Grzegorza Węgrzyna, genetyka z Uniwersytetu Gdańskiego, to wcale nie jest nierealny pomysł. W końcu i tu, i tu, dochodzi do gromadzenia się w komórkach pewnych substancji…
Mama kilkuletniej dziewczynki przesyła film, gdzie córka do tej pory prawie niemówiąca, zaczyna wypowiadać swoje imię i mówić: „mama”. Chłopiec, który miał siostrę chorą na chorobę spichrzeniową, został od razu przebadany i zdiagnozowano u niego taką samą wadę genetyczną. Kiedy miał pół roku, zastosowano u niego podwójne leczenie, genisteiną i enzymatyczne. W tej chwili kończy podstawówkę i jest zupełnie normalnym chłopcem. Co czuje profesor i jego zespół po dwudziestu latach pracy w laboratorium, kiedy otrzymuje takie informacje?
Rzeczywiście, ponad 20 lat pracujemy nad chorobami spichrzeniowymi. Najbardziej cieszę się, że można tym dzieciom pomóc. Młodzi członkowie zespołów, którymi kieruję, mówią, że dla nich takie wieści to najwspanialsza nagroda. Czujemy satysfakcję, gdy dziecko mniej cierpi, gdy dorosły człowiek ma jakąś nadzieję. Chłopiec bez leku byłby obecnie w stanie bardzo ciężkim. Jego dobre samopoczucie raczej nie jest przypadkiem. Podobnie ta dziewczynka, która po kilku latach zaczyna mówić, nie jest przypadkiem. Bierze udział w eksperymencie medycznym, ale ten nie prowadzi do rejestracji leku. Pokazuje zaś, czy substancja działa czy nie. Przeprowadzenie eksperymentu jest zasługą Stowarzyszenia Pacjentów NBIA, którzy wszystko sfinansowali. Ale też prof. Magdalena Chrościńska-Krawczyk z Lublina była zdeterminowana, żeby eksperyment zorganizować.
Chorób genetycznych jest ok. 20 tys., w tym 7 tys. stanowią jednogenowe. Każda z nich jest rzadka, ale jeśli je zsumujemy to jest 30 milionów ludzi chorych w USA, drugie tyle w Europie. Wraz z chorym cierpią całe rodziny.
Bał się pan tego eksperymentu?
Nie! Nauka nie polega na testowaniu jakiś „wziętych z księżyca” pomysłów. Nauka to mozolne dochodzenie do weryfikowalnych doświadczalnie wniosków, zatem nie ma się czego bać – trzeba się starać zrozumieć zjawisko, proces, mechanizm. Oczywiście, nigdy nie możemy być pewni, że coś zadziała zgodnie z hipotezą. W tym przypadku eksperyment medyczny był poprzedzony długimi badaniami w laboratoriach. Wiedzieliśmy też, że genisteina jest bezpieczna, bo była już testowana pod tym kątem w Stanach Zjednoczonych. Duże dawki podawano dzieciom przez rok, a niektórym przez dwa lata. Nic złego nie stało się. Pytanie brzmiało, czy ten lek zadziała efektywnie w przypadku pacjentów, a nie tylko w badaniach na komórkach czy w testach na zwierzętach. Ale ponieważ dziewczynka nie miała innej alternatywy…
Co to za grupa chorób, nad którymi pracujecie?
To choroby genetyczne, których wspólną cechą jest to, że w wyniku błędu genetycznego, mutacji, pojawiają się w komórkach różnego rodzaju substancje, które nie mogą się rozkładać. Gromadzą się więc albo wytrącają w postaci tzw. agregatów. W chorobie Huntingtona jest to zmutowane białko huntingtyna, źle się zwija i wytrąca się z roztworu.
Gdy rozbijemy jajo kurze, widzimy płynne białko i tak powinna wyglądać nasza komórka. Jeśli podgrzejemy białko, ono ścina się, wytrąca. Podobny proces dzieje się w chorych komórkach, oczywiście, nie pod wpływem temperatury, tylko pod wpływem czegoś, co sprawia, że białko źle się fałduje. Białko w jajecznicy wytrąca się, właśnie dlatego, że się źle fałduje. W przypadku chorób, o których mówimy, przyczyną „złego fałdowania” jest mutacja i wynikająca z niej zaburzona struktura białka – ale efekt jest taki sam. Jeśli mamy w organizmie takie komórki „z jajecznicą” w środku, a nie z roztworem, one nie mogą funkcjonować. Taki proces dotyka pojedynczego białka. Potrzeba więc miesięcy bądź lat, żeby ono nagromadziło się w komórce na tyle, żeby ją całkowicie zapchać.
Czyli większość chorób spichrzeniowych nie daje od razu objawów?
W chorobie Huntingtona widać je po 30-40 latach, mukopolisacharydoza, czy choroba Sanfilippo daje pierwsze objawy po kilkunastu miesiącach, choroba NBIB - po kilku do kilkunastu miesięcy. Normalnie w komórkach odbywa się proces, który wszystko, co nieprawidłowe usuwa – bo od czasu do czasu, nawet u zdrowego człowieka, jakieś białko źle się zwinie albo jakieś organellum komórkowe jest uszkodzone, wtedy też trzeba je usunąć.
Mówi pan o procesie autofagii?
Tak, to ten proces powoduje usuwanie niewłaściwych struktur. Tylko że jeśli jest ich zbyt dużo, proces jest za mało wydajny. Działanie genisteiny polega na uaktywnieniu tego procesu, żeby komórka pozbyła się złogów. Przy złogu tworzy się pęcherzyk, otaczający go, łączy się z organellami – lizosomami. A to są z kolei pęcherzyki wypełnione enzymami trawiennymi. Trawią wszystko, co jest w środku.
Trawią niezależnie od tego, czy to „wszystko w środku” jest dobre dla organizmu czy niedobre?
Tak. I właśnie tu dochodzimy do clou problemu. Wykorzystanie autofagii w pozbywaniu się niepotrzebnych substancji z komórki, nie jest naszym pomysłem. Znane są skuteczne aktywatory tego procesu, bardzo mocno go stymulują. Tyle że świetnie działają w laboratorium, ale jeśli przesadzimy z efektywnością autofagii, komórka sama siebie zje. Leku stymulującego autofagię używa się przy przeszczepach. Ale można go przyjmować krótkoterminowo, najlepiej dwa tygodnie, do miesiąca. Po tym czasie nastąpi przestymulowanie komórki i ona zje samą siebie, a efekty uboczne będą tragiczne. Problem z chorobami genetycznymi, którymi się zajmujemy, neurodegeneracyjnymi, polega na tym, że one będą trwały do końca życia. Nie naprawimy w każdej komórce defektu genetycznego, nie pozbędziemy się niepotrzebnych złogów przez miesiąc i później możemy odstawić lek. To tak nie działa.
Jeśli przerwie się podawanie leku, znów gromadzą się złogi?
Tak. Wszystko wraca bardzo szybko. W związku z tym trzeba było znaleźć coś, co da bodziec do autofagii, ale będzie na tyle łagodne, żeby komórka nie zjadła samej siebie. I właśnie przez te 20 lat poszukujemy substancji, która by w ten sposób działała. Mamy genisteinę - stymuluje autofagię, ale do pewnego momentu, nie przesadza.
To są bardzo skomplikowane mechanizmy, które przedstawiłem w prosty sposób, żeby mogli je zrozumieć nie tylko biochemicy. Genisteina to związek z grupy izoflawonów.
A co z genisteiną na chorobę Alzheimera?
Kilka lat temu opublikowaliśmy artykuł „Jeden lek na wiele chorób”. Jeśliby na jedną chorobę rzadką szukać leku, nie będzie chciał nikt go produkować. Chorób rzadkich jest kilkanaście tysięcy. Natomiast 70 proc. chorób neurodegeneracyjnych jest spowodowanych różnymi złogami. Jeśliby więc znaleźć jedną substancję radzącą sobie ze wszystkim złogami, rozwiązalibyśmy problem chorób rzadkich, neurodegeneracyjnych. Genisteina sobie radzi. W chorobie Huntingtona likwiduje złogi huntingtyny, w przypadku choroby Alzheimera likwiduje złogi beta-amyloidu, ale też białka tau i paru innych związków, które się odkładają.
W przypadku choroby Alzheimera firmy farmaceutyczne poszły w ślepą uliczkę – poszukiwały jednego celu. Oczywiście, taki jednocelowy lek jest najłatwiej przebadać, opatentować i zarejestrować. O ile w chorobach jednogenowych wiemy, co może być celem, aczkolwiek te choroby nie są do końca tak proste, jak nam się wydawało, o tyle choroba Alzheimera jest wywoływana nie tylko przez beta-amyloid. Niestety, publikacja pokazująca go jako głównego sprawcę choroby, zrobiła dużo złego. Beta-amyloid jest owszem ważnym, ale nie jest jedynym związkiem, który się odkłada. Wielu naukowców poszło w kierunku, żeby pozbyć się tylko beta-amyloidu: szukali enzymów, przeciwciał. Jedyny zarejestrowany na razie na Alzheimera lek to właśnie te specyficzne przeciwciała. Obniża poziom beta-amyloidu, ale nie daje efektów klinicznych, tzn. pacjenci, jak byli chorzy, tak są chorzy.
Dlaczego tak się dzieje?
W badaniach szło dobrze, a jednak lek nie działa. W laboratorium najczęściej chorobę Alzheimera bada się na modelach zwierzęcych. Wstrzykuje się beta-amyloid do mózgu myszy albo konstruuje się genetycznie zmodyfikowane myszy takie, żeby produkowały bardzo dużą ilość beta-amyloidu. Objawy są podobne jak u chorych na Alzheimera. Tylko że u tych zwierząt beta-amyloid jest jedyną przyczyną choroby. Jeśli ją zniwelujemy czy przeciwciałami czy czymkolwiek innym, jest dobrze. A u ludzi beta-amyloid jest jedną z wielu przyczyn. To tak jak z samochodem, który ma cztery opony przebite. Naprawimy jedną, a on i tak dalej nie pojedzie. My proponujemy substancję, która ma przewagę, bo genisteina stymuluje autofagię tak, że zniszczy wszystko, co jest odłożone. Nasz zespół wykonał doświadczenia na modelu szczurzym. Chorobę Alzheimera wywoływaliśmy, podając gryzoniom toksynę do mózgu. W tej chwili przeprowadzamy doświadczenia na myszach genetycznie zmodyfikowanych. Mają gromadzące się beta-amyloid i białko tau, znów model niepełny, ale jednak dwubiałkowy. Podajemy im genisteinę, żeby sprawdzić, czy zadziała na tym modelu genetycznym.
Oby działało. Uszczęśliwilibyście starzejące się społeczeństwa.
Tyle że znów spotykamy się z problemem, co dalej. Na zwierzętach poszło nam dobrze. Która jednak firma farmaceutyczna zechce wyłożyć pieniądze? Żeby były próby kliniczne, trzeba takiej determinacji, jaką wykazało się wspomniane na początku stowarzyszenie, które robi eksperyment medyczny na swój koszt.
Gdy się wpisuje w wyszukiwarkę „prof. Grzegorz Węgrzyn”, wyskakuje hasło Sanfilippo. Coś więcej o tej chorobie?
Zajęliśmy się nią jako pierwszą z chorób spichrzeniowych. To choroba z grupy mukopolisacharydoz. Specyficzne cukry, glikozoaminoglikany, odkładają się w komórkach, bo brakuje enzymu, który je rozkłada. Znów atakujemy chorobę genisteiną. Z jednej strony stymuluje ona autofagię, z drugiej spowalnia syntezę cukrów, które nie mogą się rozłożyć. To bardzo ładnie wychodzi na komórkach i na zwierzętach. W USA były robione próby kliniczne pierwszej fazy i pokazały bezpieczeństwo tego leku. Druga próba robiona w Holandii pokazała, że spada poziom glikozoaminoglikanów. Była też zrobiona próba kliniczna III fazy z kontrolą placebo w Wielkiej Brytanii. Niestety, odbyła się tylko w jednym ośrodku, a więc na zaledwie 19 pacjentach, bo brakowało sponsora. Połowa dostawała genisteinę, połowa placebo. Ale choroba Sanfilippo ma to do siebie, że postępuje. Pierwsze objawy pojawiają się w wieku 2-4 lat, im dalej, tym gorzej, bo jest neurodegeneracja. Pacjentów jest mało, żyją około 20 lat, a ostatnie lata życia to już naprawdę terminalna wegetacja, choć wcześniej jako dzieci są hiperaktywne. Potem są odżywiane sondą. Ucieszyłem się, gdy jeden chory dożył 29 lat.
Dużo jest chorych na Sanfilippo?
W Polsce kilkadziesiąt dzieci, na świecie kilka tysięcy. Grupę badaną w Wielkiej Brytanii tworzyły trzylatki, które prawie nie miały objawów i osiemnastolatki w stanie terminalnym. Próba kliniczna musi pokazać, co się polepszyło. W naszej próbie pokazano, że obniża się poziom tego, co się spichrza, ale nie wykazano istotnych statystycznie efektów klinicznych.
Dlaczego?
Jeśli mamy trzylatka praktycznie bez objawów, któremu podajemy lek, on może mu troszkę pomoc, ale to nie będzie ogromna różnica, bo dziecko jest jeszcze w bardzo dobrej formie. Jeśli podamy lek osiemnastolatkowi w stanie terminalnym, on już jest tak zdegenerowany, że nagle nie stanie i nie będzie normalnie funkcjonował. Jak w takiej grupie kontrolnej pokazać statystycznie istotną poprawę? Próba więc w sensie statystycznym nie powiodła się. Teraz będzie ciężko namówić jakąś firmę, żeby się tym zajęła.
Dużo się dziś mówi na temat antybiotykooporności, ale wy i na tym polu macie osiągnięcia. Urząd Patentowy przyznał zespołowi naukowców z Wydziału Biologii UG oraz Instytutu Biochemii i Biofizyki PAN cztery patenty na wynalazek wykorzystujący bakteriofagi do zapobiegania infekcjom u ludzi i zwierząt oraz zwalczania tych infekcji?
Antybiotykooporność to kolejny duży problem medyczny. Projektem terapii fagowej kieruje moja żona, prof. dr hab. Alicja Węgrzyn. Gdy w 1928 r. Fleming odkrył penicylinę, wydawało się, że mamy panaceum na wszystkie bakteryjne choroby. Niestety, bakterie nabierają oporności na różnego rodzaju antybiotyki, a my zaczęliśmy ich bardzo nadużywać.
Polacy są liderami w Europie.
Ale daleko nam do Chin czy Indii. Zresztą, nadużywanie w medycynie to kropla w morzu. Problemem są antybiotyki w hodowli zwierząt.
Zwierzęta je wydalają, my zjadamy…
W biologii jest selekcja – tak przebiega ewolucja. Jeśli dajemy środek, który zabija bakterie, przeżywają tylko te, które są oporne na niego. Bardzo skutecznie więc selekcjonujemy szczepy bakteryjne, które wytworzyły albo nabyły oporność na antybiotyki. Efekt jest taki, że już w tej chwili są na świecie szczepy bakterii oporne na wszystkie znane antybiotyki, a ich lista rozszerza się. WHO alarmuje, że jeśli nie znajdziemy alternatywy dla antybiotyków, w 2050 r. każde skaleczenie, najmniejsza operacja chirurgiczna będzie zagrożeniem życia. Dziś przy zabiegu chirurgicznym podajemy antybiotyk i nie ma sepsy.
Jedną z alternatyw jest zastosowanie wirusów specyficznych dla bakterii - bakteriofagów. Wirus wchodzi do komórki, namnaża się, rozbija ją i „wychodzi” jego „potomstwo”. Problem polega na tym, że bakteriofagi są specyficzne nie tylko do gatunków, ale też do szczepów bakterii. Żeby mieć skuteczną terapię fagową, nie wystarczy mieć 10 bakteriofagów – trzeba wyizolować ich setki albo tysiące, żeby zobaczyć, który z nich w chwili zakażenia zaraża bakterię i wtedy go zastosować albo najlepiej koktajl dwóch, trzech szczepów bakteriofagów, bo wtedy jest szansa, że nie pojawi się mutant oporny na tyle szczepów. I właśnie terapią wśród zwierząt zajmuje się fagowa grupa żony. Jeśli bowiem wyeliminujemy całkowicie antybiotyki z hodowli drobiu, bydła czy trzody chlewnej, zwierzęta padną. We Wrocławiu w Instytucie Immunologii i Terapii Doświadczalnej PAN jest grupa robiąca eksperymentalną terapię fagową u ludzi. Ale i z tą terapią jest problem prawny. Żeby wprowadzić na rynek lek, musi być bardzo dokładna charakterystyka chemiczna danego związku. Tu lekiem jest wirus. Owszem, można wszystkie jego białka i genom sekwencjonować, ale jak to zrobić dla tysiąca szczepów? To tak drogie i nieopłacalne, że nikt nie jest w stanie tego udźwignąć. Dlatego Unia Europejska dyskutuje nad zmianą prawa. Te dyskusje nie mogą trwać długo, bo mamy naprawdę problem antybiotykooporności. Oczywiście, charakterystyka fagów musi być, ale nie aż tak dokładna.
Skąd u pana i pana żony zainteresowanie genetyką?
Genetyką interesowaliśmy się od dawna. Natomiast za zainteresowaniem chorobami genetycznymi stoi osobisty powód. Nasza córka cierpiała na chorobę z grupy mukopolisacharydoz, konkretnie typu I… Genetycy i chora córka…
Nie żyje. Podawaliśmy jej genisteinę. Oprócz tego miała terapię enzymatyczną wymagającą cotygodniowych wlewów. Robiły się zrosty. Wszczepiliśmy port. Ola miała go pięć lat i wymagał wymiany. W czasie operacji okazało się, że ma rzadkie uczulenie na plastik. Spuchła. Wyjęto port, zrobiono tracheotomię. Rurka tracheotomiczna to też plastik…
Ola zmarła 9 lat temu w wieku prawie 16 lat. Los z nas zadrwił. Powtarzała nam, że trzeba być dzielnym, nie płaczemy więc, pomagamy innym dzieciom, innym ludziom. Nie robimy tego dlatego, żeby lepiej się czuć. Zresztą nie pracujemy przecież sami, tylko wraz z zespołami naukowców – te osoby są tak samo zaangażowane w badania, bez nich niewiele można by zrobić. To one przez długie godziny pracują codziennie w laboratoriach. Bez Karoliny, Lidki, Magdy, Zuzi, Estery i innych mógłbym co najwyżej pomarzyć o ważnych odkryciach. Naprawdę chcemy pomóc, wiemy, z jakimi problemami borykają się rodziny dzieci z chorobami rzadkimi. Nikt ich nie rozumie, każdy patrzy, że mają dziwne dzieci, nie ma leczenia, znikąd pomocy. Oczywiście, nie daję rodzicom nadziei, że wyleczymy każdą chorobę, ale jeśli dziecko ustabilizuje się i nie będzie pogorszenia, to już sukces.
Rozmawiała Beata Igielska, zdrowie.pap.pl